Super-sectioning with multi-sheet reversible saturable optical fluorescence transitions (RESOLFT) microscopy
著者: Andreas Bodén, Dirk Ollech, Andrew G. York, Alfred Millett-Sikking, Ilaria Testa
ライトシート蛍光顕微鏡(LSFM)は、低いレーザー照射量で迅速な3次元イメージングを可能にするため、多細胞システムの4D細胞イメージングにおいて貴重なツールである。特に、広範囲の試料に対して薄い照明シート(約2〜5μm)を作成することが比較的容易であり、背景光を低減しつつ良好なセクショニング能力を提供する。また、複数の発光シートを並列に作成することにより、超解像セクショニング能力(<100nm)を達成することができ、さまざまな細胞構造を高精度で追跡することが可能である。
しかし、従来のLSFMは、シート幅が広いため、特に生細胞内の微細な細胞内情報を取得するのが困難である。例えば、従来のLSFMでは、試料の厚さに対して照明シートが比較的厚く(>1μm)、小さな細胞内構造(約1〜10μm)の詳細なセクショニングが制限される。また、特殊なパターン化や光スイッチング遷移を使用して薄い照明シートを作成する試みがなされているが、生物学的タイムラプスイメージングにおいては、フォトンの検出効率が低く、試料のアクセス性が悪く、光スイッチングが最適でないため、実際の時空間分解能が低下する。
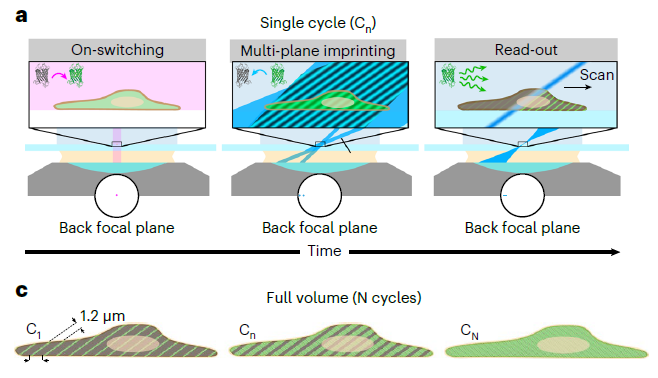
そこで、本研究では、可逆飽和光蛍光遷移(RESOLFT)技術を利用し、並列化されたスイッチングスキームを採用して、従来のシステムよりも最大10倍薄いシートを励起し、超解像セクショニング能力を実現した。具体的には、リバーシブルスイッチング蛍光タンパク質(RSFP)を使用し、広視野オンスイッチング照明とオフスイッチングパターンを組み合わせることで、多層の発光シートを作成し、0.4〜0.6kHzの速度で迅速に読み出した。この技術により、1ボリュームあたり10〜20回のスイッチングサイクルのみで、140×84×15μm³のボリュームイメージングが可能となり、細胞分裂、アクチンの動き、ウイルス様粒子のダイナミクスなどの細胞プロセスを追跡することができた。また、従来のLSFMと比較して、より薄い照明シート(<200nm)を使用することで、細胞構造の高精細なボリューム記録を実現し、細胞内の動的な構造を詳細に観察することができた。
Cobolt社のレーザー発振器の仕様と実験内容
使用したライトシートは、ファイバーカップリングされたCobolt 488nm, 200mWレーザーで、コリメートされたビームはスリットを通過して調整された。照明に組み込まれた光学系により、資料に対して最適な照明パターンが形成され、様々な光スイッチングプロトコルがなされた。