Maryam, S., Venkata Sekar, S.K., Ghauri, M.D., Fahy, E., Saito Nogueira, M., Lu, H., Beffara, F., Humbert, G., Ni Riordain, R., Sheahan, P., Burke, R., Kho, K.W., Gautam, R., Andersson-Engels, S. “Mobile multi-configuration clinical translational Raman system for oral cancer application.” Analyst 2023, 148, 1514-1523.
背景
口腔がんの早期診断は患者の生存率を大幅に向上させるために極めて重要である。口腔がんは一般的に進行した段階で発見されることが多いため、初期段階での検出が生存率を劇的に向上させる可能性がある。ラマン分光法は非侵襲的な技術であり、分子情報を詳細に提供できるため、がんの早期診断に有望である。また、生体液や生体組織の分析に適しており、水が弱い散乱体であるため、他のスペクトル技術と比べて干渉が少ないという利点があり、診断の精度と信頼性が向上する。したがって、ラマン分光法を用いた新しい診断システムの開発は、口腔がんの早期発見と治療において重要な役割を果たす可能性がある。
従来の問題点
しかし、従来のラマン分光法は、信号が非常に弱いため高感度の検出器が必要であり、高額な設備が必要となる。また、従来のラマン分光システムは大型で非ポータブルであり、臨床環境での使用には適していない。
解決方法の提案と実験結果
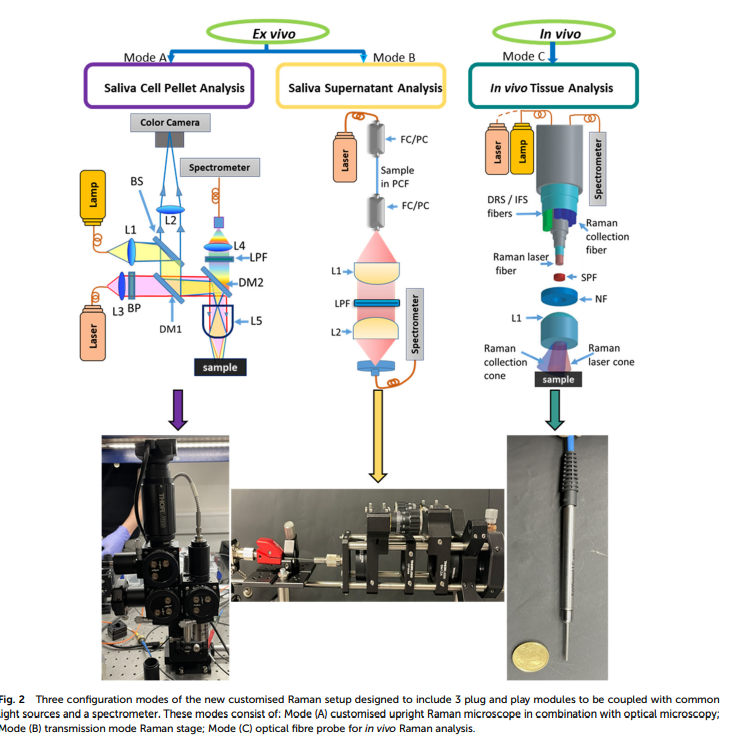
そこで、本研究では、多構成のカスタマイズされたラマンシステムを開発し、3つの異なる構成でのin vivoおよびex vivo分析を可能にすることによって、これらの問題を解決した。具体的には、モード(A)では細胞ペレットのラマン信号を高い信号対雑音比で取得する顕微鏡を使用し、モード(B)では液体サンプルの低濃度分析のための新しい長経路透過セットアップを設計し、モード(C)では口腔組織からのin vivoデータを収集するためのマルチモーダルファイバー光学プローブを使用した。このシステムは、Cobolt社製のレーザー(785 nm、Cobolt 08-01シリーズ)を光源として使用しており、高い帯域抑制能力を持つ。また、このシステムはコンパクトでコスト効果が高く、容易に輸送可能であり、臨床手順にシームレスに統合できる。これにより、初期の口腔がんの完全なスクリーニングが可能となり、診断の精度と信頼性が向上する。最終的には、ラマン分光法のデータ収集と解析が自動化され、さらに効果的な診断ツールとなることが期待される。
論文で使用された785nmレーザー
